
复旦大学丁建东教授课题组借助RUIDU自主研制的超声喷涂系统,对聚乳酸PLA涂层的质量进行了很好的控制,成功制备出了可加速铁基生物材料降解的金属-聚合物复合支架。为生物可降解材料的研究提供了新的思路,为生物可降解心血管支架的开发提供了一种简单的候选技术。
实验方案

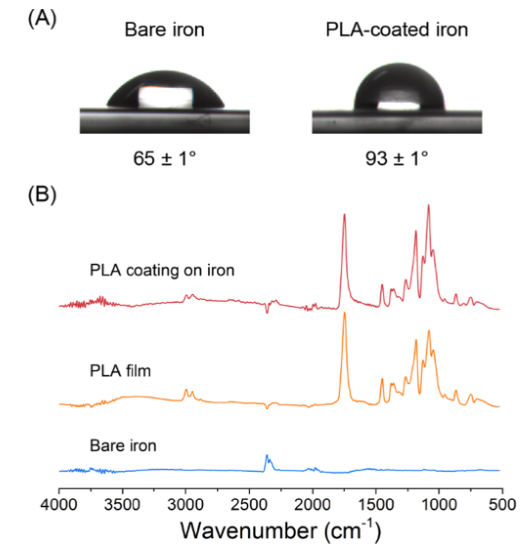
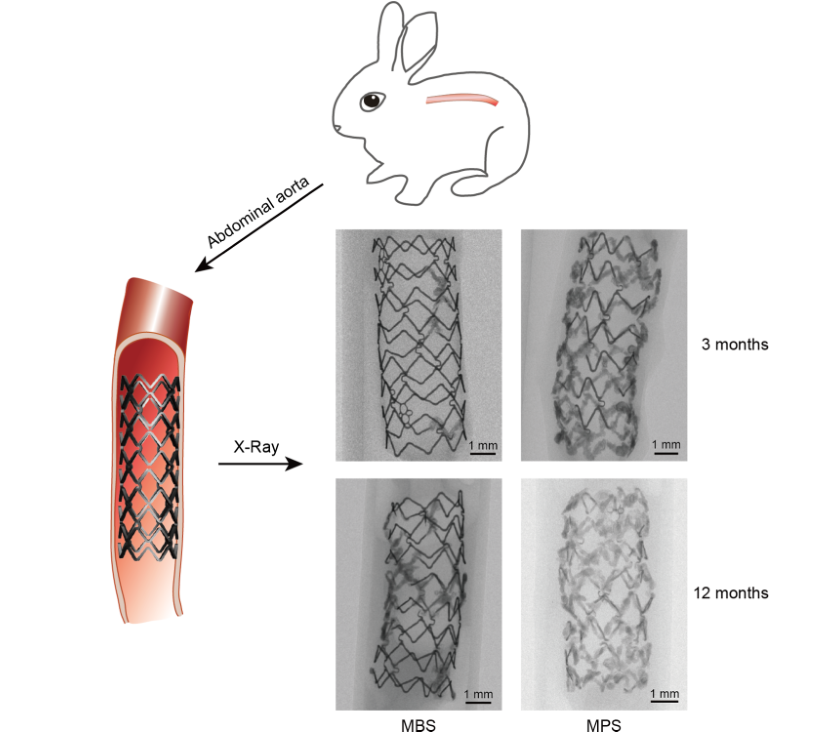
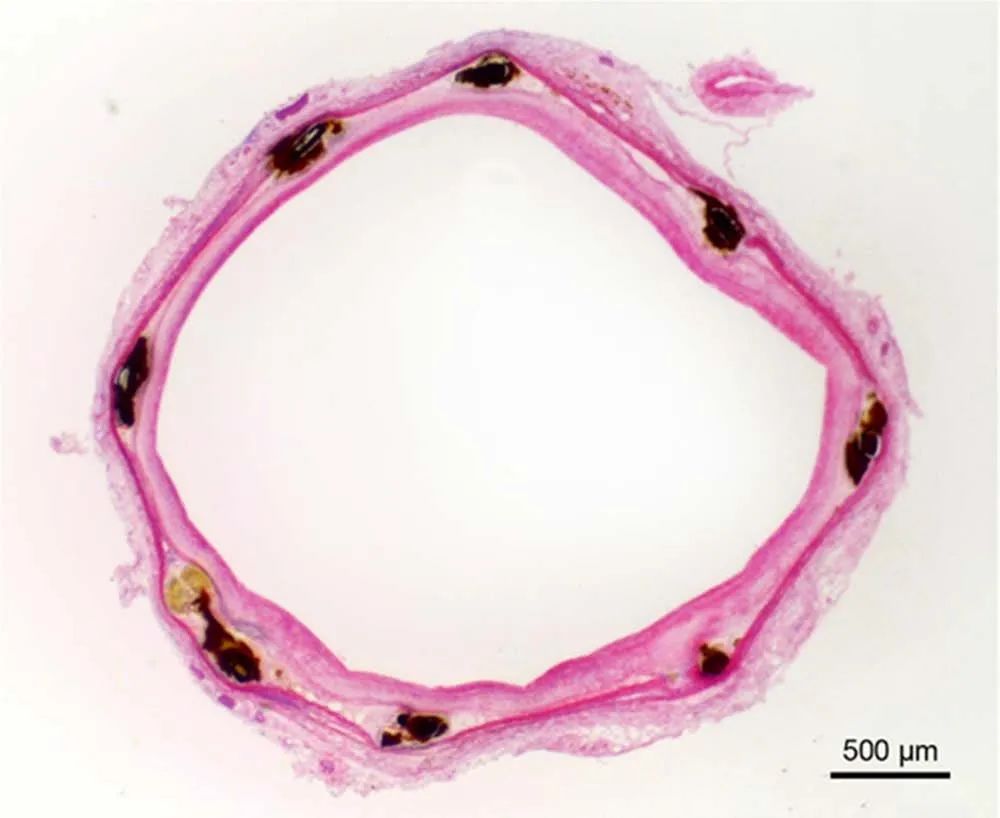
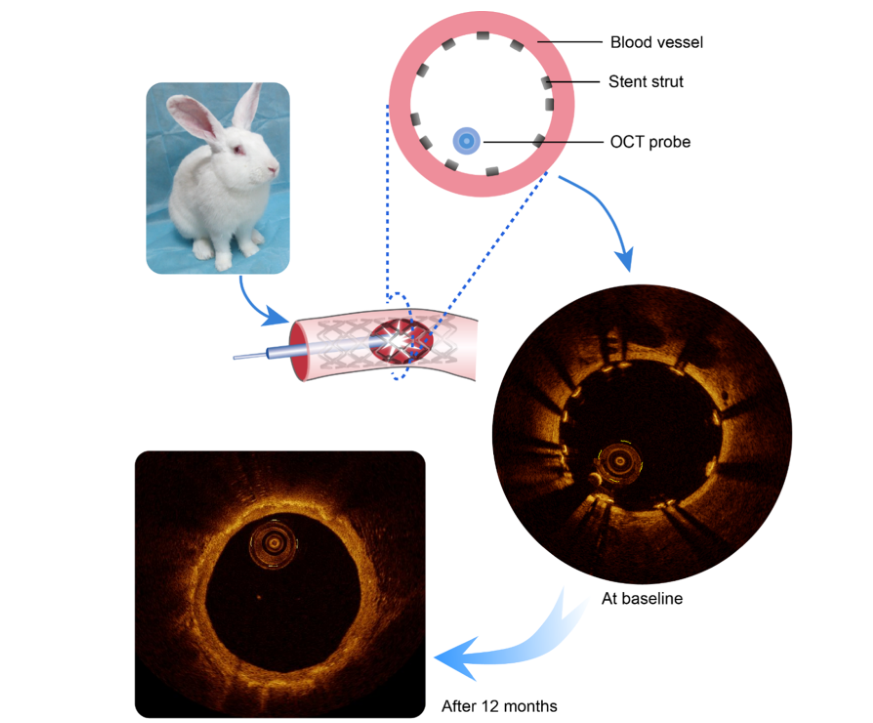
参考文献:
Yongli Qi, Haiping Qi, Yao He, et al. Strategy of Metal−Polymer Composite Stent To Accelerate Biodegradation of Iron-Based Biomaterials[J]. ACS Appl. Mater. Interfaces 2018, 10, 182−192
